


新版《医药工业洁净厂房设计规范》 GB50457-2008 将于2009-06-01 正式施行。本规范 从原有国家医药管理局内部规范升级为国家规范。新增加了许多强制性条款。(黑粗体表示)
适用范围:新建、扩建和改建的医药工业洁净厂房
编写基础:
医药洁净室(区)的空气洁净度等级
| 悬浮粒子最大允许数(个/m3)≥0.5um | FDA GMP | 中国 GMP | EU GMP + WHO | ISO |
|---|---|---|---|---|
| 3,520 | 100 | 100 | A(关键部位) | 5 |
| 35,200 | 1,000 | 1,000 | B(洁净室背景,动态百级) | 6 |
| 352,000 | 10,000 | 10,000 | C | 7 |
| 3,520,000 | 100,000 | 100,000 | D | 8 |
| 10,500,000 | 300,000 |
洁净室测定状态:
WHO—-静态+动态
工艺无特殊要求下,洁净区温湿度:
| 空气洁净度等级 | 温度℃ | 相对湿度% |
|---|---|---|
| 100 | 20~24℃ | 45~60% |
| 10,000 | 20~24℃ | 45~60% |
| 100,000 | 18~26℃ | 45~65% |
| 300,000 | 18~26℃ | 45~65% |
| 人员净化 | 16~20℃(冬) 26~30℃(夏) | 无要求 |
### 建议值
温度:
夏季:
冬季:
相对湿度:
压差:
| 高级别洁净区与低级别洁净区 | >5Pa (国外 10Pa) |
|---|---|
| 洁净区与非洁净区 | >5Pa (国外 10Pa) |
| 洁净区与室外 | >10Pa (国外 15Pa) |
照度:
| 主要生产区 | 300lx |
|---|---|
| 辅助区,走廊,人物流洁净 | 150lx |
| 特殊工段 | 按工艺要求设局部照明 |
噪音:
| 非单向流洁净室(空态) | <60dB(A) |
|---|---|
| 单向流、混合流洁净室(空态) | <65dB(A) |
原则:
| 药品生产厂房类型 | 布置要求 | 解释 |
| 青霉素等高致敏性药品的厂房 | 独立设置 | 独立建筑物,与其他建筑物之间的道路、空地、绿化等隔开。 建筑物之间的间距必须符合《建筑设计防火规范》。 建筑物之间不能有任何连接(包括走廊)。 |
| 避孕药品 | 分开设置 | 可在同一建筑物内,但生产区域之间实墙分隔到顶。两者之间无任何人员、物料、净化空 调系统风管等之间的联系。仅仅在火灾情况下可以借用邻近区域的走道及出入口作为疏散 通道用。 实墙---分隔到顶、无开空、无门窗(疏散门除外)的墙体 |
| 卡介苗 | ||
| 结核菌素 | ||
| 抗癌药品 | ||
| Β-内酰胺 | 分开布置 | 同一建筑物内,根据不同生产品种和工艺流程,划分成不同的生产区域。 可以是同一建筑物同一楼层的不同区域,也可以是同一建筑的不同楼层。 其人员总更衣、内部联系走、仓库、空调机房、工艺用水设备等均可共用,但药品生产操作岗位及辅助设施(空调系统)均需独立设置不得共用。 尤其对进入暴露工序的人员净化更衣设施,必须独立设置。 非暴露工序(外包)也不得共用。 |
| 中药材的前处理,提取,浓缩等生产区与其制剂生产区 | ||
| 动物脏器,组织的洗涤处理生产区与其制剂生产区 | ||
| 含不同核素的放射性药品 |
以下生物制品的原料和成品不得在同一生产区加工灌装
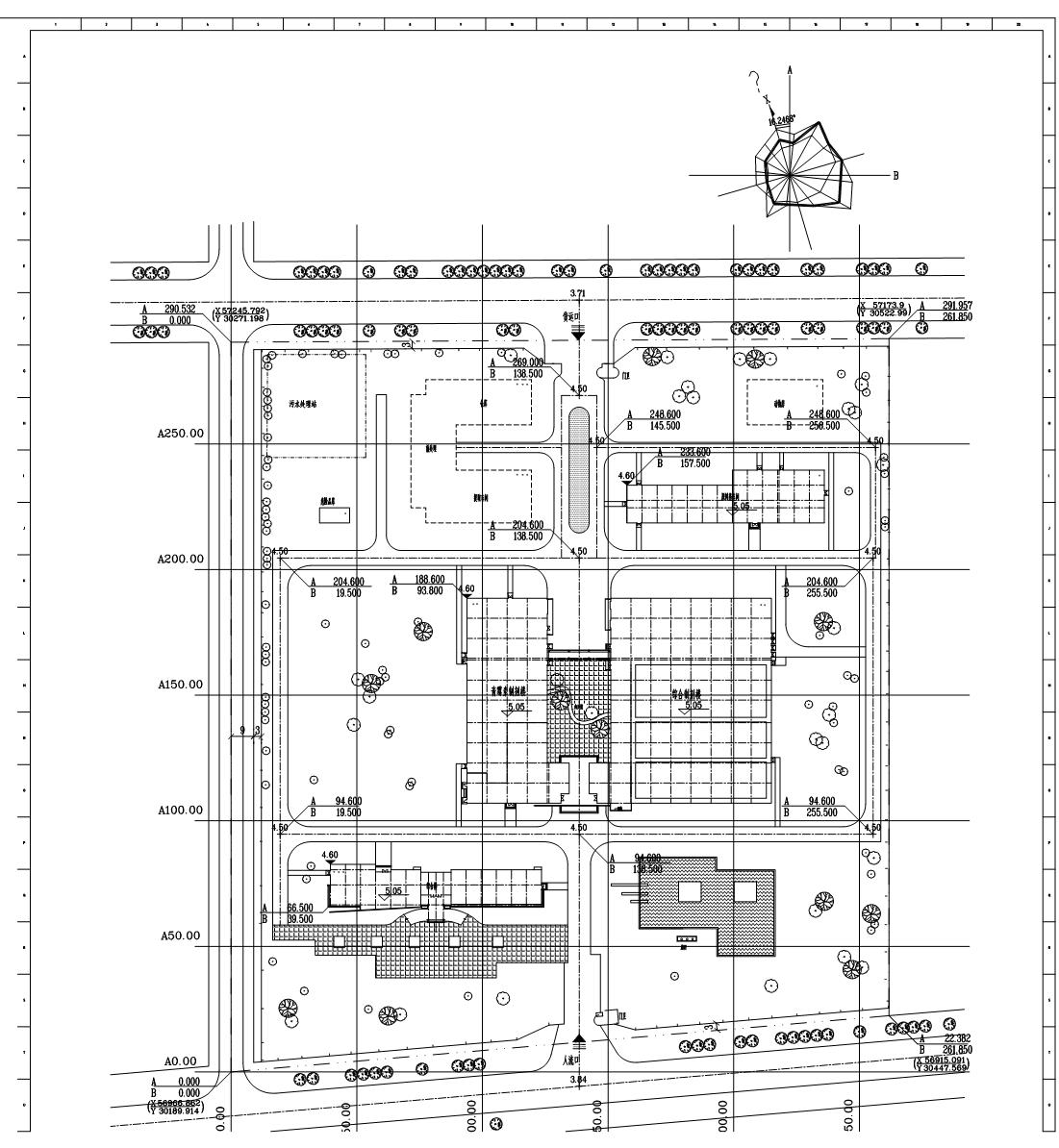
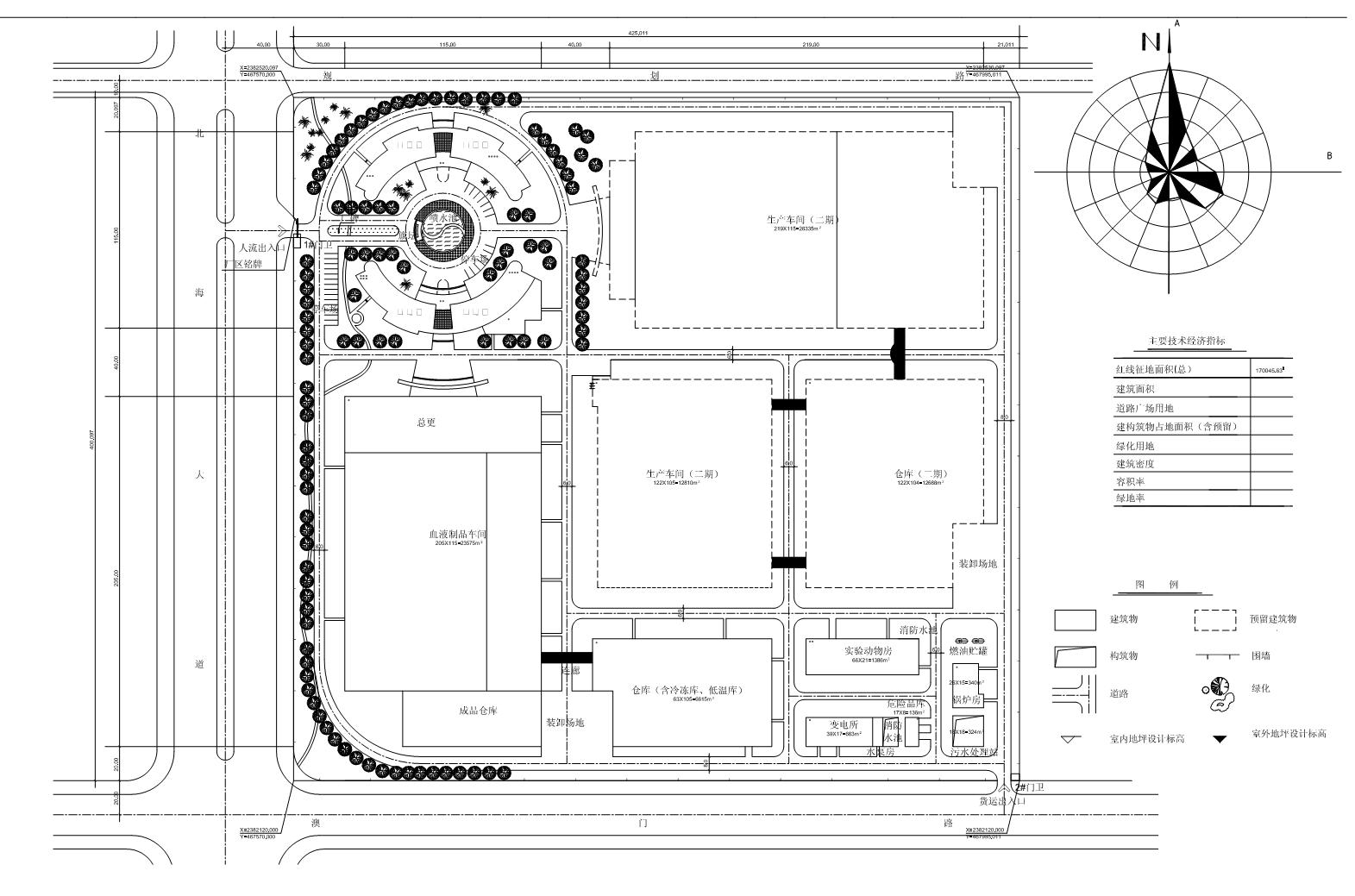
5.1.2 工艺布局应防止人流和物流之间的交叉污染,应符合下列基本要求:
5.1.9 生产辅助用室的布置和空气洁净度等级
1. 取样室

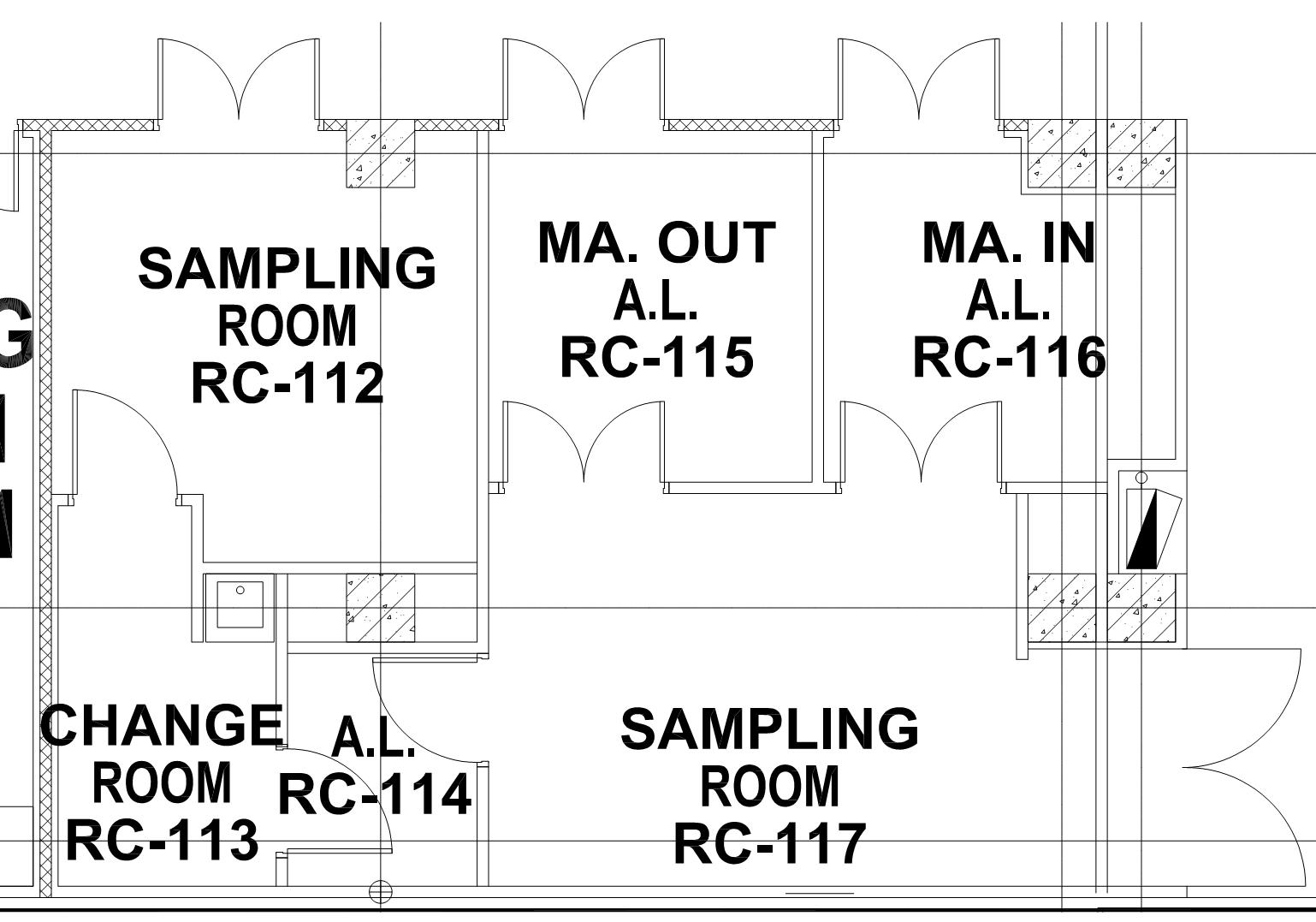
2. 称量室称量室宜设置在生产区内,称量室的空气洁净度等级应与使用被称量物料的医药洁净室(区)相同。称量区必须保证待称量物料称量完毕的物料不会混淆特殊药品的称量区必须独立设置称量区需注意除尘、压差控制。有条件应采用称量柜。
3. 备料室备料室宜靠近称量室布置,备料室的空气洁净度等级应与称量室相同。
4. 清洗室
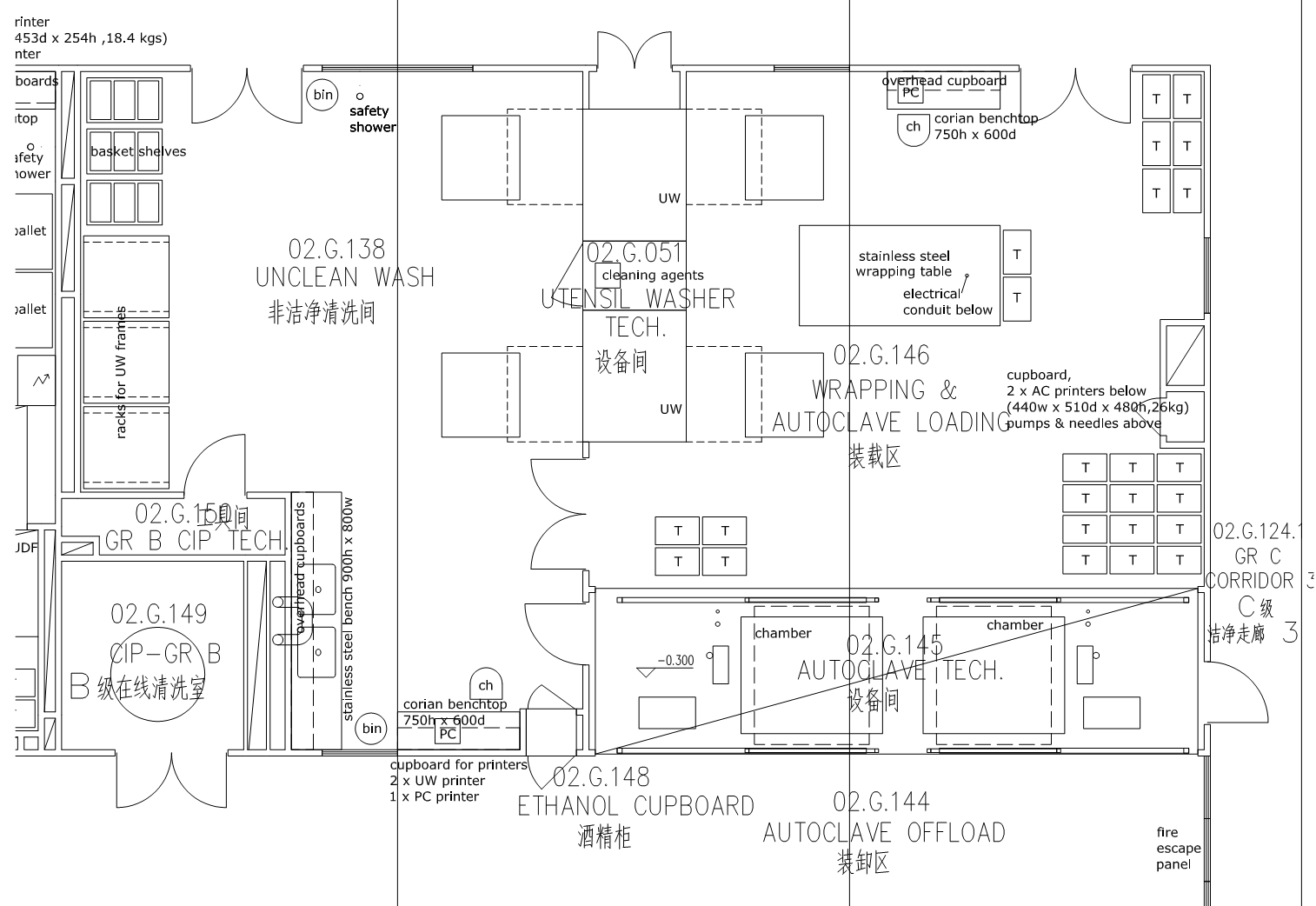
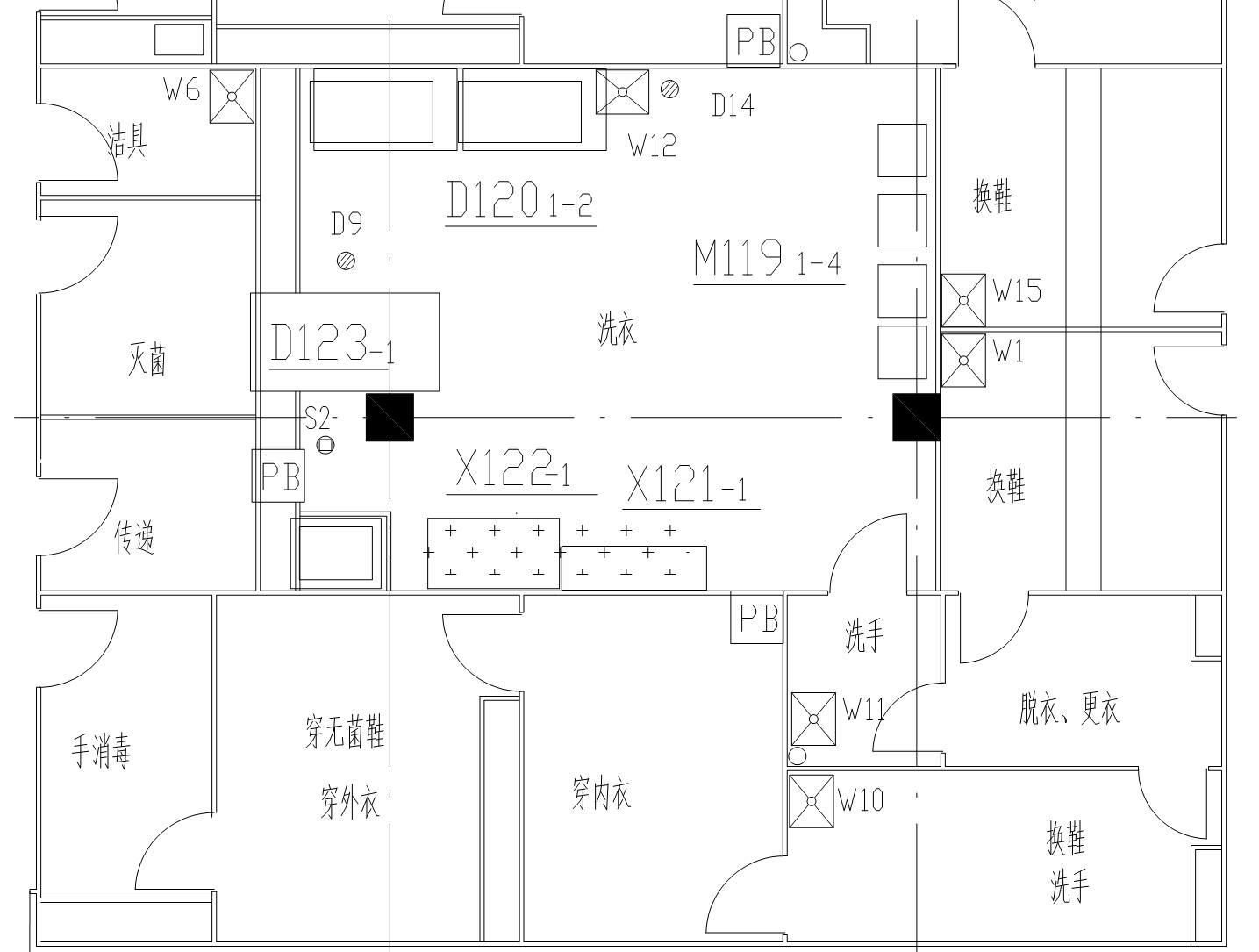
5.1.11 洁净工作服洗涤、干燥和整理
1. 空气洁净度100000级及以上的医药洁净室(区)的洁净工作服洗涤、干燥和整理室,空气洁净度不应低于300000级。
100000级空气洁净度:洗涤—干燥—整理—使用
2. 空气洁净度300000级的医药洁净室(区)的洁净工作服可在清洁环境下洗涤和干燥。
普通环境:洗涤—干燥—整理—使用
3. 不同空气洁净度等级的医药洁净室(区)使用的工作服,应分别清洗、整理。(洗衣房可集中设置,但不宜同时在一个洗衣机内洗)。
4. 无菌工作服的洗涤和干燥设备宜专用。洗涤干燥后的无菌工作服应在空气等级100级单向流下整理,并应及时灭菌。
100000级空气洁净度:洗涤—烘干—100级层流下整理、包装—蒸汽湿热灭菌—无菌生产区使用
5. 特殊药品工作服清洗场合及设备必须独立。
5.1.13 质量控制实验室
5.1.15 医药工业洁净厂房应设置防止昆虫和其他动物进入的设施空气幕杀虫灯隔离带
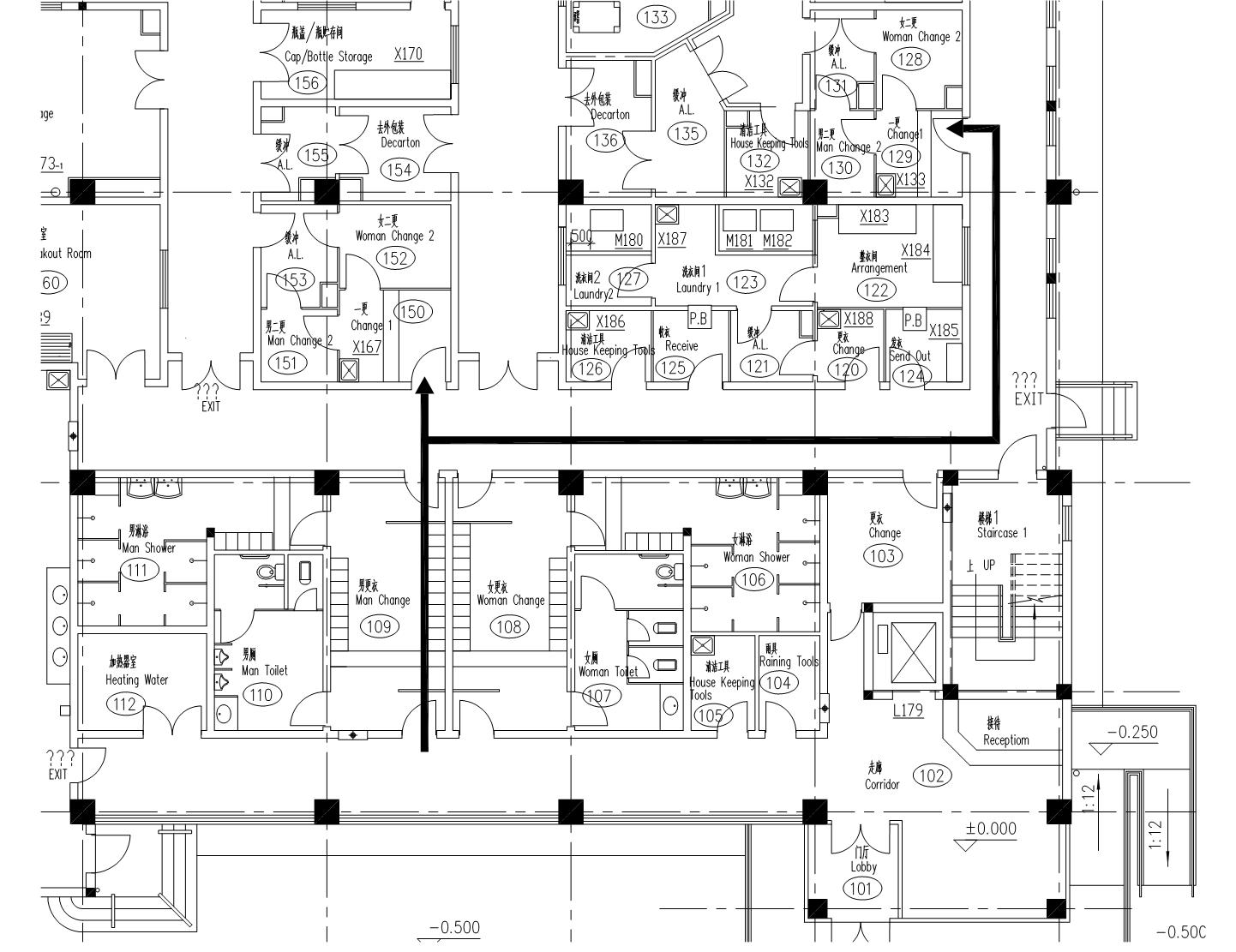
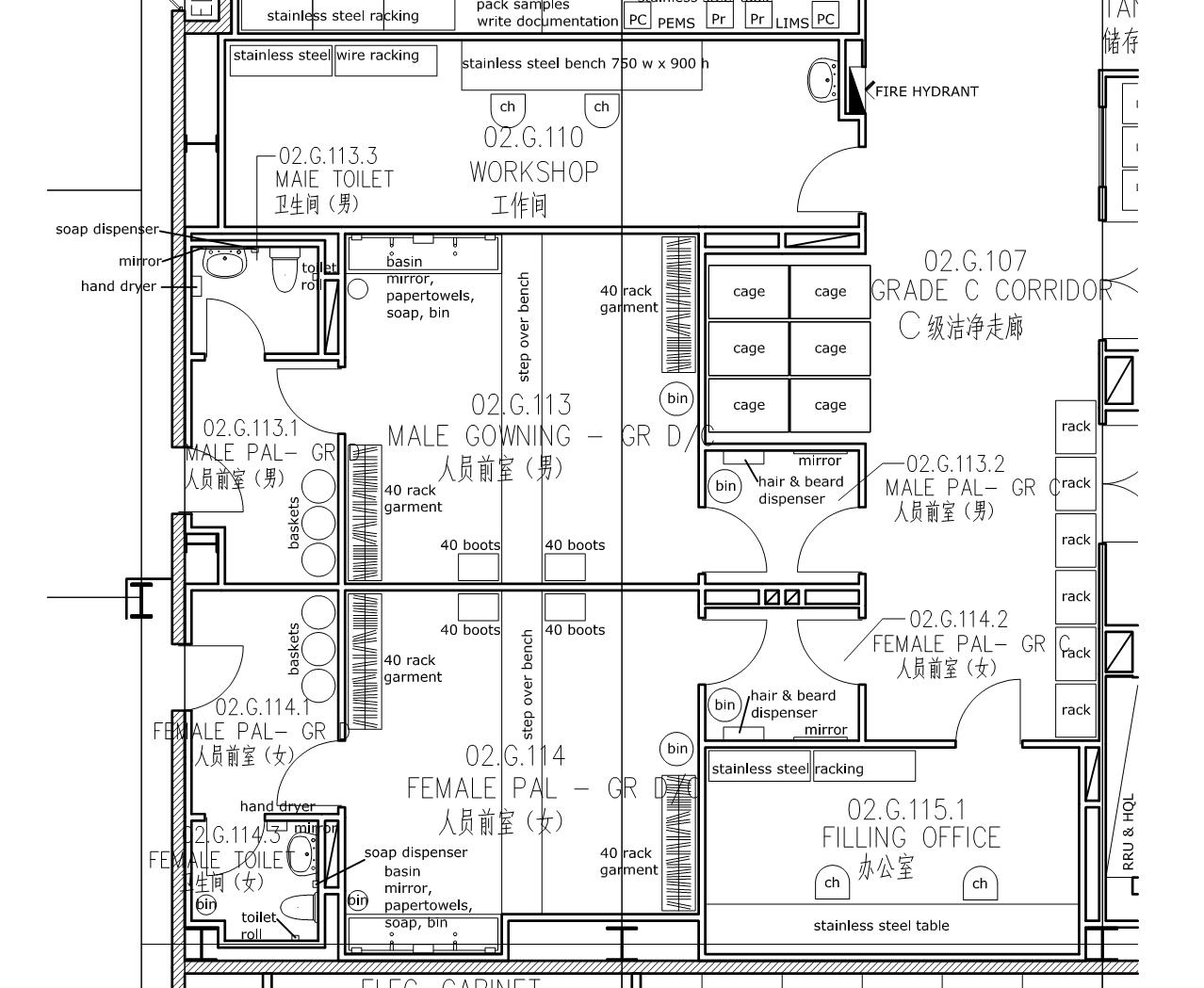
5.2.1 医药工业洁净厂房内人员净化用室和生活用室的设置
5.2.2 人员净化用室和生活用室的设计
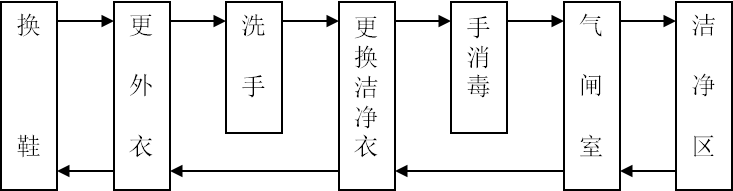
5.2.4 医药工业洁净厂房内人员净化程序
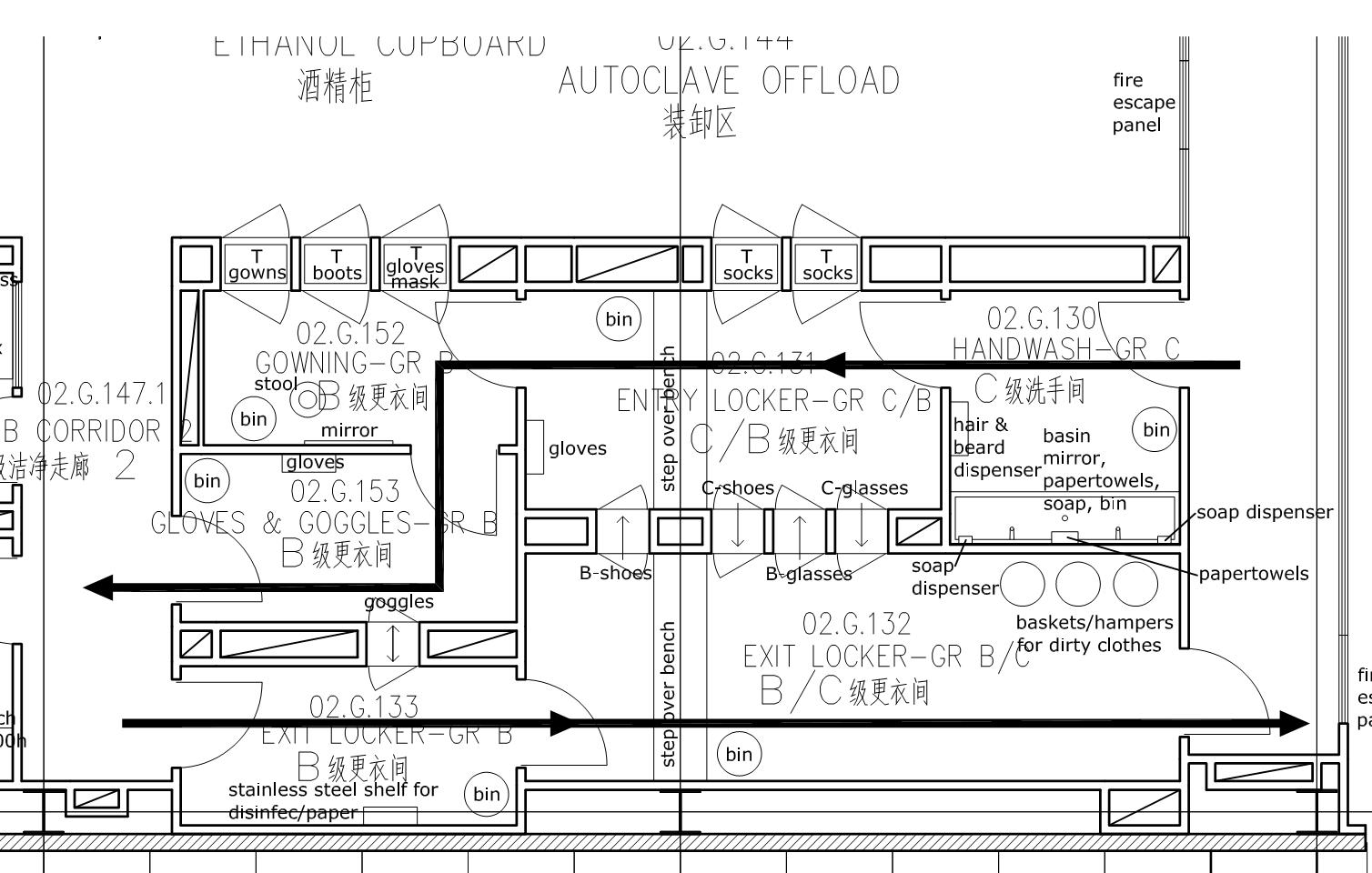
5.3.1 医药洁净室(区)的原辅物料、包装材料和其他物品出入口,应设置物料净化用室和设施。
5.3.2 进入无菌洁净室(区)的原辅料、包装材料和其他物品,除满足本规范5.3.1的规定外,尚应在出入口设置供物料、物品灭菌用的灭菌室和灭菌设施。(风淋传递柜配合紫外线)
5.3.3 物料清洁室或灭菌室与医药洁净室(区)之间,应设置气闸室或传递柜。
5.3.5 生产过程中产生的废弃物出口,以单独设置专用传递设施,不宜于物料进口合用一个气闸室或传递柜。
| 纯化水 | 注射用水 | |||||
| 中国药典 | 美国药典 | 欧盟药典 | 中国药典 | 美国药典 | 欧盟药典 | |
| 电导率 | —— | 符合规定 | <1.3us/℃m | —— | 符合规定 | <1.1us/℃m |
| 总有机碳 | —— | <0.5mg/l | <0.5mg/l | —— | <0.5mg/l | <0.5mg/l |
| 内毒素 | —— | —— | <0.25EU/ml | <0.25EU/ml | <0.25EU/ml | <0.25EU/ml |
| 微生物 | <100℃fu/ml | <100℃fu/ml | <100℃fu/ml | <100℃fu/ml | <100℃fu/ml | <100℃fu/ml |
纯化水:纯化水输送管道系统应采取循环方式。设计和安装时不应出现使水滞留和不易情节的部位。循环的干管流速宜大于1.5m/s,不循环的支管长度不应大于管径的6倍。
注射用水:注射用水输送管道系统应采取循环方式。注射用水的贮存可采用65℃以上保温循环的方式,也可采用80℃以上或4℃以下保温的方式。循环时干管流速宜大于1.5m/s。
6.1.1 医药洁净室(区)内因少敷设管道。工艺管道的干管宜敷设在技术夹层或技术夹道。需要拆洗和消毒的管道宜明敷。易燃、易爆、有毒物料管道应明敷,当需穿越技术夹层时,应采取安全密封措施。
6.1.4 工艺管道的干管系统应设置吹扫口、防净口和取样口。
6.1.9 可燃气体和氧气管道的末端或最高点应设置发送能放散管。引至室外的放散管应高出屋面1m,并应采取防雨和防异物侵入措施。
6.4.1 存放及使用易燃、易爆、有毒介质设备的放散管应引至室外,并应设置相应的阻火装置、过滤装置和防雷保护设施。
6.4.2 输送易燃介质的管道,应设置导除静电的接地设施。
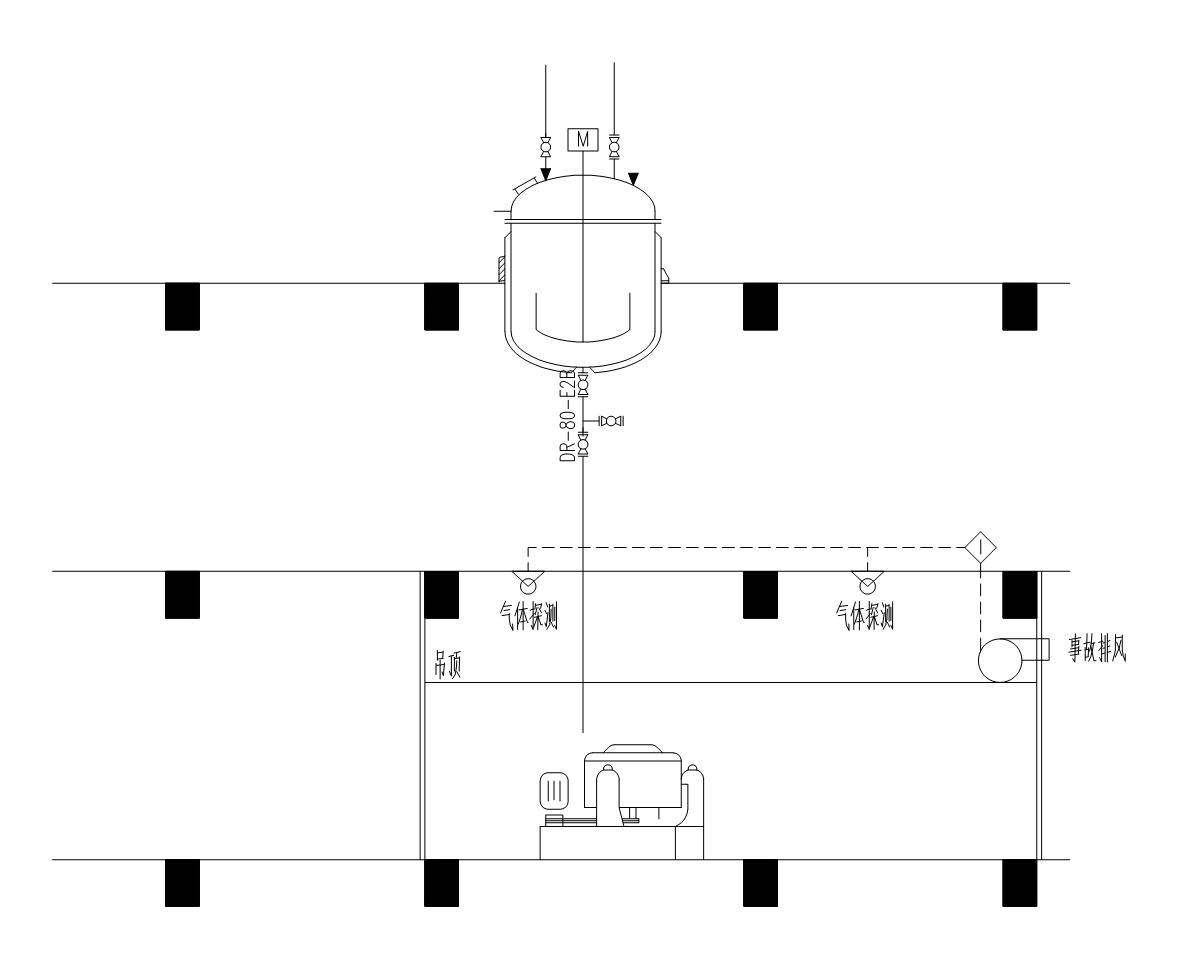
6.4.3 下列部位应设置易燃、易爆介质报警装置和事故排风装置,报警装置应与相应的事故排风装置连锁。
6.4.5 各种气瓶应集中设置在医药洁净室(区)外。当日使用气量不超过一瓶时,气瓶可设置在医药洁净室内,但必须采取不积尘和易于清洁的措施。
7.1.7 空气洁净度10000级的医药洁净室(区)使用的传输设备不得穿越较低级别的区域。
7.1.8 医药洁净室(区)内的各种设备均应选用低噪声产品。对于辐射噪声值超过洁净室容许值得设备,应设置专用隔声设施。(空态60dB)
7.1.9 医药洁净室(区)与周围工程楼内强烈振动的设备及其管道连线时,应采用主动隔振措施。有精密设备、仪表仪器的医药洁净室(区),因根据各类振源对其影响采取被动隔振措施。
7.2.12 特殊药品的生产设备:
8.2.1 医药工业洁净厂房的耐火等级不应低于二级。
8.2.3 医药洁净室(区)的顶棚和壁板(包括夹芯材料)应采用非燃烧体,且不得采用燃烧时产生有害物质的有机复合材料。顶棚的耐火极限不应低于0.4h,壁板的耐火极限不应低于0.5h,疏散走道的顶棚和壁板的耐火极限不应低于1.0h。
8.2.4 技术竖井井壁采用非燃烧体,其耐火极限不应低于1.0h。井壁上的检查门的耐火极限不应低于0.6h,竖井内各层或间隔一层楼板处,应采用与楼板耐火极限相同的非燃烧体作水平防火分隔,穿越水平防火分隔的管线周围空隙,应采用耐火材料紧密填堵。
8.2.5 医药工业洁净厂房每一生产层、每一防火分区或每一洁净区的安全处出口数目不应少于二个,但符合下列要求可设一个:
8.2.6 安全出口应分散设置,从生产地点至安全出口不应经过曲折的人员净化路线,并应设置疏散标志,安全疏散距离应符合现行国家标准《建筑设计防火规范》GB50016的有关规定。
8.2.8 医药洁净厂房及医药洁净室(区)同层外墙应设置供消防人员通往厂房洁净室(区)的门窗,门窗的洞口间距大于80m时,应在该段外墙设置专用消防口。
专用消防口的宽度不应小于750mm,高度不应小于1800mm,并应设置明显标志。楼层的消防口应设置阳台,并应从二层开始向上层架设钢梯。
举例(窗,隔断圆角,门,门框不宜设门槛,安全门可,技术夹层宜设检修走道,上人吊顶行走有挤压变形)

9.1.3 医药洁净室(区)内的新鲜空气量,应按下列最大值:
最大值的确定
1. 送风量
| 空气洁净度等级 | 气流流型 | 平均风速(m/s) | 换气次数(次/h) |
|---|---|---|---|
| 100 | 单向流 | 0.2~0.5 | – |
| 10,000 | 非单向流 | – | 15~25 |
| 100,000 | 非单向流 | – | 10~15 |
| 300,000 | 非单向流 | – | 8~12 |
换气次数适用于层高小于4m医药洁净室(区),室内人员少,发尘少,热源少时宜采用下限值。
2. 根据热、湿负荷计算确定的送风量
3. 向医药洁净室内供给的新鲜空气量
洁净室的换气次数:
9.2.1 空气洁净度100级、10000级、100000级的空气净化处理,应采用粗效、中效、高效空气过滤器三级过滤。空气洁净度300000级的空气净化处理、,可采用亚高效空气过滤器。
9.2.5 下列情况的净化空气调节系统的空气不应循环使用:
9.2.8 医药洁净室(区)的排风系统,应符合下列规定:
9.2.9 采用熏蒸消毒灭菌的医药洁净室(区),应设置消毒排风设施
9.2.10 下列情况排风系统,应单独设置:
9.2.11 人员更衣室的净化空调设计
除进入医药洁净室(区)的气闸室空气洁净等级与相连的医药洁净室(区)空气洁净度等级相同外,其他人员净化用室中各个房间均不列级,用送入洁净空气的风量来控制其洁净要求。
9.2.14 放散大量有害气体或有爆炸气体的医药洁净室(区)应设置事故排风装置,事故排风系统应设置自动和手动控制开关,手动控制开关因分别设置在洁净室(区)内的洁净室(区)外便于操作的地点。
9.2.15 医药工业洁净厂房疏散走廊应设置排风设施。
9.2.18 下列医药洁净室(区)应设置指示压差的装置:
9.2.19 下列医药洁净室(区)应与相邻医药洁净室(区)保持相对负压。
9.2.20 质量控制实验室净化空调的设置
9.6.2 青霉素等特殊药品的精制、干燥、包装室及其制剂产品的分装室的室内应保证正压,与相邻房间或区域之间应保持向对付负压。
9.6.4 青霉素等特殊药品生产区的空气均应经高效空气过滤器过滤后排放。二类危险度以上病原体操作区及生物安全室,应将排风系统的高效空气过滤器安装在洁净室(区)内的排风口处。
10.3.1 医药工业洁净厂房的排水系统,应根据生产排出的废水性质、浓度、水量等确定。有害废水应经废水处理,达到国家排放标准后排出。
10.3.2 医药洁净室(区)的排水设备以及与重力回水管道相连接的设备,必须在其排出口以下部位设置水封装置,水封高度不应小于50mm。排水系统应设置透气装置。
10.3.3 排水立管不应穿过空气洁净度100级、10000级的医药洁净室(区);排水立管穿越其他医药洁净室(区)时,不应设置检查口。
10.3.4 空气洁净度100级的医药洁净室(区)内不应设置地漏。
10.4 消防设施
符合《建筑设计防火规范》GB 50016-2006
11.2.7 医药工业洁净厂房内应设置备用照明,并应满足所需场所或部位活动和操作的最低照明。(为减少灯具重复设置,节省投资,备用照明可作为正常照明的一部份)
11.3.3 医药工业洁净厂房的生产区(包括技术夹层)等应设置火灾探测器。医药工业洁净厂房生产区及走廊应设置手动火灾报警按钮。
11.3.4 医药工业洁净厂房应设置消防值班室或控制室。消防值班室或控制室不应设置在医药洁净室(区)内。消防值班室或控制室应设置消防专用电话总机。
11.3.6 医药工业洁净厂房中易燃、易爆气体的贮存、使用场所应设置气体监测器。报警信号应联动启动或手动启动相应得事故排风机,并应将报警信号送至控制室。
11.4.3 医药洁净室(区)的净化空气调节系统,应采取防静电接地措施。
11.4.4 医药洁净室(区)内产生静电危害的设备、流动液体、气体或粉体管道应采取防静电接地措施。
11.4.6 医药工业洁净厂房的防雷接地系统设计应符合现行国家标准《建筑物防雷设计规范》GB50057的有关规范。
© 2025 河北筑邦净化设备安装工程有限公司